Bibliografía
Recipiente: Ha de ser de vidrio ó de plástico, y de medio litro de capacidad para poder realizar análisis completos.
Toma de muestras: Es importante que la muestra sea representativa y que pase el menor tiempo posible entre la toma y el análisis para evitar alteraciones en la composición.
Embalaje: Una vez que la muestra se encuentra en el recipiente y este cerrado hermeticamente, se recubriran tapon y cuello con tela ó papel fuerte-, y despues se remitiran al laboratorio acompañada de una hoja descriptiva ( Origen del agua, nombre del pozo ó paraje, toponimia del lugar, etc..).
Se entiende como tal el sumatorio de todos los iones con carga positiva que se determinan en un análisis de aguas.
Para obtener dicho sumatorio se tienen en consideración los siguientes cationes: Calcio [Ca2+], Magnesio [ Mg2+], Sodio [Na+], Potasio [K+ ] y Amonio [NH4+].
De igual forma se establece para los iones con carga negativa. Siendo éstos: Cloruro [Cl-], Sulfato [SO4=], Bicarbonato [CO3H-], Carbonatos [CO32-], Nitrato [NO3-], Nitrito [NO2-] y Fosfato [PO43-].
La suma de los aniones ha de coincidir aproximadamente con la de los cationes, expresados ambos sumatorios en meq/l.
Se permite un error del 20 % por exceso o por defecto, considerándose en este caso el análisis como correcto.
Para comprobar si el análisis es correcto también se puede usar esta relación, así pues, la suma de cationes, expresada en meq/l., multiplicada por un coeficiente que oscila entre 80 y 110, debe coincidir con el valor numérico de la conductividad eléctrica expresada en dS/m.
El pH de un análisis tiene que estar entre un intervalo de 7 - 8. Con estos valores el agua analizada se considera "normal".
El contenido total de sales está relacionado con la conductividad eléctrica de la muestra mediante la siguiente expresión:
S.T. = C.E. x K
Siendo:
- S.T.: Concentración en sales totales.
- C.E.: Conductividad eléctrica de la muestra a 25º C.
- K.: Constante de proporcionalidad. Fijándosele a ésta un valor aproximado de 0,64 si la conductividad eléctrica se expresa en dS/m y el contenido en sales totales en ppm o lo que es igual, en mg./l.
|
CE (dS/m) |
BAJO |
MEDIO |
ALTO |
|
F.A.O. |
CE < 0.75 |
0.8 < CE < 3.0 |
CE > 3.0 |
Se evalúa por la presencia y concentración de iones fitotóxicos disueltos en el agua, y que una vez en el suelo representan un grave riesgo para la planta.
|
IONES (g/l) |
BAJO |
NORMAL |
ALTO |
|
Cloruro (Cl-) |
Cl- < 0.3 |
0.3 < Cl- < 0.7 |
Cl- > 0.7 |
|
Sulfato (SO4)-2 |
(SO4)-2 < 1.0 |
1.0< (SO4)-2 < 1.5 |
(SO4)-2 > 1.5 |
|
Sodio (Na+) |
Na+ < 0.2 |
0.2 < Na+ < 0.6 |
Na+ > 0.6 |
Se refiere a la proporción relativa en que se encuentran el ión sodio y los iones calcio y magnesio, expresada su concentración en meq/l. Pretende ser una medida del poder de degradación de la estructura del suelo por su contenido en sodio.
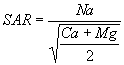
Cuando su valor es inferior a 10, el agua se considera como "no alcalinizante".
Se calcula de la forma siguiente:
RASajus = RAS x (1+ (8,4 - pHc))
Donde:
pHc = (pk2 - pkc) + p (Ca 2+ + Mg 2+ ) + p (Alk )
(pk2 - pkc) = f (Ca 2+ + Mg 2+ + Na + )
p (Ca 2+ + Mg 2+ ) Se calcula en tablas.
p (Alk ) = f (CO3 2- + HCO3- )
|
S.A.R.adj |
NORMAL |
MEDIO |
ELEVADO |
|
F.A.O. |
SARadj <3 |
3 < SARadj < 9 |
SARadj > 9 |
Es otro índice de la acción degradante del agua. Las concentraciones de los diferentes iones se expresan en meq/l.
C.S.R. = [CO2-] + [CO3H-] - [Ca2+] - [Mg2+]
| |
CSR (meq/l) |
|
RECOMENDABLES |
CSR < 1.25 |
|
POCO RECOMENDABLES |
1.25 < CSR< 2.50 |
|
NO RECOMENDABLES |
CSR > 2.50 |
El grado de dureza se refiere al contenido en calcio de las aguas. Se expresa en grados hidrotimétricos franceses (G.H.F.).
G.H.F. = ([Ca2+] * 2,5 + [Mg 2+] * 4,12)/10
|
TIPO DE AGUA |
Grados Hidrométricos Franceses |
|
Muy Dulce |
ºF < 7 |
|
Dulce |
7 < ºF < 14 |
|
Medianamente dulce |
14 < ºF < 22 |
|
Medianamente dura |
22 < ºF < 32 |
|
Dura |
32 < ºF < 54 |
|
Muy dura |
ºF > 54 |
Este índice valora la calidad agronómica de un agua en función de las concentraciones entre ion cloruro, sulfato y sodio, pudiendo definirlo como la altura del agua, expresada en pulgadas (2.54 cm) que después de la evaporación dejaría en un terreno vegetal, de cuatro pies de espesor, aproximadamente 1.2192 m, álcali suficiente para imposibilitar el desarrollo normal de las especies vegetales más sensibles.
Es decir, en realidad este coeficiente K, evalúa la toxicidad que pueden producir las concentraciones de los iones cloruro y sulfato, aportadas con el agua de riego y que permanecen en el suelo tras formar cloruro y sulfato de sodio respectivamente. El cálculo de este índice, se basa por tanto en los tres siguientes axiomas:
I.- Si |Na+| - 0.65*|Cl-| = 0 valor negativo;
entonces:
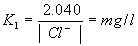
II.- Si: |Na+| - (0.65*|Cl-|) es positivo, pero no mayor que (0.48 *|SO4-2| )
entonces:
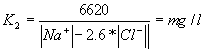
III.- Si |Na+| - (0.65*|Cl-|) - (0.48 *|SO4-2| ) = valor positivo;
entonces:
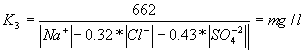
Por tanto expresado en meq/l, si:
Cl- > Na+ ; entonces Índice de Scott = K1
Cl- < Na+ < SO4-2 ; Índice de Scott = K2
Cl- > Na+ + SO4-2 ; Índice de Scott = K3
|
Valor de K (K1,K2 o K3) |
CALIDAD DEL AGUA |
|
Buena |
K > 18 |
|
Tolerable |
18 >K >6 |
|
Mediocre |
6 > K > 1.2 |
|
Mala |
K < 1.2 |
La precipitación del calcio en el agua puede ser anticipada mediante el Indice de Saturación de Langelier, según el cual, el carbonato de calcio precipita cuando alcanza su límite de saturación en presencia de bicarbonato. Este índice se define por la diferencia entre el pH actual del agua pHa y el pH teórico que el agua alcazaría en equilibrio con el CaCO3 (pHc):
Indice de sauración = pHa - pHc
Se calcula el pHc, con la única diferencia respecto al RASaj que el segundo sumando sólo se tiene en cuenta la concentración de Ca2+ y no la de ( Ca 2+ + Mg 2+ ).
pHc= ( pk2-pkc ) + p( Ca 2+ + p ( Alk ))
El Indice de Langelier ( Is ) es la diferencia entre el pH del agua y el pHc.
Ayers, R.S. y D.W. Westcot. 1985. Water quality for agriculture. FAO Irrig. and Drain. Paper Nº 29, Roma.
Cánovas, J. 1986. Calidad agronómica de las aguas para riego. Ministerio de agricultura pesca y alimentación. Madrid.
Cerda A., Caro M. y Fernandez F.G. 1980. Criterios básicos para evaluar la calidad de las aguas para riego. An . Edaf. Agrob. XXXIX. 1779-1791.
Pescod, M.M. 1992. Wastewater treatment and use in agriculture. FAO Irrig. & Drain. Paper No. 47, Roma.
Maas, E.V. 1990. Crop salt tolerance. En: Agricultural salinity assessment and management. K.K. Tanji (ed), Am. Soc. Civil Eng., Manual & Rep. on Eng. nº 71, New York, pp. 262-304.
Nakayama F.S. y D.A. Bucks. 1991. Water quality in drip/trickle irrigation: A review. Irrigation Sci. 12: 187-192
Organización Mundial de la Salud. 1989. Directrices sanitarias sobre el uso de aguas residuales en agricultura y acuicultura. Informe Técnico 778. OMS, Ginebra.